Marzia Giaccardi, Jacopo Giovacchini, Tania Chechi
S.C. Cardiologia, Ospedale Santa Maria Annunziata – Firenze
Abstract
Lo scompenso cardiaco rappresenta un’entità patologica di grande impatto clinico. Accanto alla terapia farmacologica, la terapia elettrica è in grado di migliorare la prognosi e la qualità di vita dei pazienti con scompenso cardiaco. A partire dalle prime intuizioni di oltre 20 anni fa da parte di un gruppo di elettrofisiologi francesi, la terapia elettrica ha conosciuto una notevole evoluzione, che attualmente affianca alla terapia di resincronizzazione anche la stimolazione fisiologica e la terapia di modulazione della contrattilità cardiaca.
Parole chiave: scompenso cardiaco, resincronizzazione, stimolazione fisiologica, modulazione, contrattilità cardiaca.
______________________________________________________________________________
Circa 1 milione di persone in Italia sono affette da scompenso cardiaco e, di queste, approssimativamente il 50% muore entro 5 anni dalla diagnosi. Dopo ogni ricovero per scompenso la funzionalità cardiaca si riduce progressivamente, ponendo l’accento sull’estrema importanza della prevenzione dei ricoveri stessi. Molti progressi sono stati fatti in termini di trattamenti farmacologici che ne hanno ridotto sia le ospedalizzazioni che la mortalità, ma il problema resta aperto e ricco di ostacoli da superare. Lo scenario terapeutico per lo scompenso cardiaco si è recentemente arricchito dall’entrata in linee guida di due nuove classi di farmaci che, alla luce dei grandi trials, hanno dimostrato di aggiungere benefici in termini di riduzione di mortalità cardiovascolare e riduzione delle ospedalizzazioni per insufficienza cardiaca rispetto alla terapia farmacologica convenzionale. Così come per i farmaci, anche la terapia elettrica dello scompenso cardiaco ha presentato negli ultimi anni diverse innovazioni. Fu un’intuizione geniale di un gruppo di elettrofisiologi francesi che, ormai più di 20 anni fa, dette vita a quella che oggi viene ritenuta il “gold standard” della terapia elettrica dello scompenso cardiaco ovvero la terapia di resincronizzazione cardiaca. Osservando quello che è il principale meccanismo fisiopatologico che porta allo scompenso cardiaco, ovvero la “desincronizzazione”, il gruppo francese sotto la guida dell’indimenticato Jacques Mugica insieme a Jean Claude Daubert, Philippe Ritter, Serge Cazeau, Daniel Gras e Philippe Mabo, trovò le soluzioni tecniche dapprima con la stimolazione epicardica chirurgica del ventricolo sinistro [FIG.1] e poi con la stimolazione epicardica raggiunta attraverso i rami del seno coronarico. Questa brillante intuizione spinse le aziende a sviluppare dispositivi ed elettrocateteri sempre più performanti al fine di raggiungere l’obiettivo prefissato ovvero la resincronizzazione atrio-ventricolare, interventricolare ed intraventricolare. Il MUSTIC fu il primo studio multicentrico randomizzato che valutò la stimolazione biventricolare con accesso transvenoso via seno coronarico e dimostrò, per la prima volta, che la resincronizzazione cardiaca migliorava la tolleranza all’esercizio, la qualità della vita e riduceva le ospedalizzazioni per scompenso. Negli anni a seguire fu dimostrato anche un beneficio in termini di riduzione di mortalità. Sappiamo bene, però, che non tutti i pazienti rispondono alla terapia di resincronizzazione cardiaca, con percentuali di “non-responders” che vanno dal 25 al 40% a seconda delle casistiche considerate. Le principali cause della mancata risposta a tale terapia si riconoscono nella selezione del paziente, nell’impossibilità di posizionare i nostri elettrocateteri per il ventricolo sinistro nelle zone target ed in scorrette programmazioni o mancate ottimizzazioni dei dispositivi. Le linee guida europee del 2021 raccomandano la terapia di resincronizzazione cardiaca in quei pazienti in ritmo sinusale, sintomatici, con frazione d’eiezione ≤35%, durata del QRS ≥ 150 msec, in presenza di blocco di branca sinistra (secondo i criteri di Strauss) nonostante sia prescritta terapia medica ottimizzata (Classe IA) al fine di migliorare i sintomi e ridurre morbilità e mortalità per scompenso. Quando la durata del QRS è tra 130 e 149 msec le linee guida suggeriscono che la terapia di resincronizzazione potrebbe essere considerata con evidenza di classe IIaB. Un’importante novità di queste ultime linee guida è l’indicazione alla terapia di resincronizzazione anche in paziente che non presentano il blocco della branca sinistra, ad oggi caposaldo dell’indicazione, purchè la durata del QRS sia ≥ 150 msec (Classe IIaB) o tra 130 e 149 msec (Classe IIbB) e presentino comunque elementi di dissincronia elettrica e/o meccanica [Tab.1]. Quando la durata del QRS è, però, <130 msec, la terapia di resincronizzazione viene considerata in classe III, ovvero nociva. Tale indicazione limita quindi l’utilizzo della terapia di resincronizzazione cardiaca solo ad un terzo dei pazienti con scompenso cardiaco. Più di due terzi dei pazienti, infatti, hanno un QRS normale (< 130 ms). Esiste quindi una fetta di pazienti affetti da scompenso cardiaco che presentano una durata del QRS< 130 msec o che sono non-responders alla resincronizzazione che necessitano di soluzioni terapeutiche alternative che affianchino la terapia medica ottimizzata. Negli ultimi anni è ritornata ad affacciarsi nella nostra pratica clinica la stimolazione fisiologica. Nata nei primi anni 2.000, non ha goduto di un grande successo iniziale fino a tempi più recenti quando, anche grazie ad importanti contributi italian,i è tornata sullo scenario clinico. La stimolazione fisiologica con il pacing Hisiano o della branca sinistra, costituisce il modo più fisiologico per stimolare il cuore. Seguendo gli insegnamenti preziosi di Albert Einstein che sosteneva come “ogni cosa che puoi immaginare la natura l’ha già creata”, a noi non resta che guardare e riprodurre ciò che la natura ha fatto per prima. Stimolare il sistema di conduzione altro non è che copiare la natura. Tale tecnica è considerata una valida alternativa, sicuramente più fisiologica, alla stimolazione del ventricolo destro. L’avvento di nuovi strumenti, quali cateteri ed introduttori dedicati, ha notevolmente facilitato gli aspetti tecnici dell’impianto, che è diventato quasi routinario in un numero crescente di centri. Il pacing fisiologico viene utilizzato al posto della stimolazione ventricolare destra, al posto della stimolazione biventricolare, oppure in associazione alla terapia di resincronizzazione. Restano aperte ancora diverse questioni che troveranno le giuste risposte nei risultati dei prossimi trials, attualmente in corso. Con più dati su sicurezza ed efficacia, è probabile che, in futuro, la stimolazione fisiologica svolgerà un ruolo crescente nella terapia di stimolazione sia convenzionale che nei pazienti con scompenso cardiaco. Un ulteriore possibile risposta terapeutica per i pazienti con scompenso cardiaco è la terapia di modulazione della contrattilità cardiaca [FIG.3] che, al momento, risulta essere l’unica efficace per i pazienti con scompenso cardiaco e QRS stretto (<130ms) sintomatici per dispnea, nonostante la terapia medica ottimale. Le recenti linee guida ESC 2021 indicano che tale terapia trova indicazione in pazienti con scompenso cardiaco con frazione di eiezione tra il 25% e il 45%, in Classe NYHA III-IV con normale durata QRS (<130 ms). La terapia di modulazione della contrattilità cardiaca prevede l’utilizzo di due elettrocateteri a fissaggio attivo che vengono impiantati nel versante destro del setto interventricolare e vengono collegati al generatore che, al pari di un comune pacemaker, viene posto in una tasca sottocutanea preconfezionata. Il generatore di impulsi impiantabile è un dispositivo programmabile con batteria interna ricaricabile e funzioni di telemetria. Viene fornito con un caricabatterie esterno, che consente al paziente di ricaricarlo settimanalmente, in modo da garantire una longevità del dispositivo fino a 20 anni. Il dispositivo funziona inviando impulsi elettrici durante il periodo refrattario assoluto del ciclo cardiaco con conseguente liberazione di ioni calcio che si rendono disponibili nel citosol e vanno ad aumentare la forza di contrazione sistolica mediante differenti meccanismi cellulari. L’effetto di tale terapia si estrinseca in tempi diversi. Una prima fase con “effetto rapido” dell’ordine di minuti-ore che prevede, appunto, il miglioramento del ciclo del calcio con aumento della forza contrattile locale in assenza di aumento del consumo di ossigeno; un “effetto intermedio” legato all’inversione dell’espressione genica fetale tipica dello scompenso cardiaco che torna all’espressione genetica normale con sintesi di proteine contrattili e riduzione della fibrosi interstiziale, con miglioramento della funzione contrattile globale, che si estrinseca da ore a settimane ed un effetto a “lungo termine” che porta ad un rimodellamento inverso dei volumi e diametri telediastolico e telesistolico del ventricolo sinistro con riduzione dello stress meccanico e neurormonale ed aumento della frazione di eiezione che si evidenzia nel giro di settimane-mesi. Questo effetto benefico avviene inizialmente solo nell’area adiacente agli elettrodi, ma con il tempo si diffonde anche in aree remote del muscolo cardiaco. I più recenti dati della letteratura riportano, oltre alle evidenze relative ai miglioramenti dei parametri clinici di tolleranza all’esercizio e di qualità di vita (miglioramento significativo della tolleranza all’esercizio valutato come variazione del pVO2 al test stress cardiopolmonare con una variazione di 0,84 ml/kg/min, miglioramento della qualità di vita valutata con il questionario Minnesota Living with Heart Failure che ha documentato un incremento di 11,7 punti, miglioramento stato clinico di scompenso valutato con indicatore NYHA che nell’81% dei pazienti migliora di almeno 1 classe vs il 42% del gruppo di controllo, miglioramento della tolleranza all’esercizio valutato con il test del 6 minuti di cammino che ha documentato una media di cammino superiore di 33,7 metri), una riduzione significativa delle ospedalizzazioni per scompenso e della mortalità, sia per pazienti in ritmo sinusale che per quelli in fibrillazione atriale. Allo stato attuale esistono molteplici gli studi in corso (5 randomizzati e più di una ulteriore decina tra non randomizzati e registri) per un totale di 1.500 pazienti arruolati. Saranno i risultati di questi studi/registri a portare ulteriori elementi di conoscenza utili a rinforzare le indicazioni all’utilizzo di tali dispositivi.
marzia.giaccardi@uslcentro.toscana.it
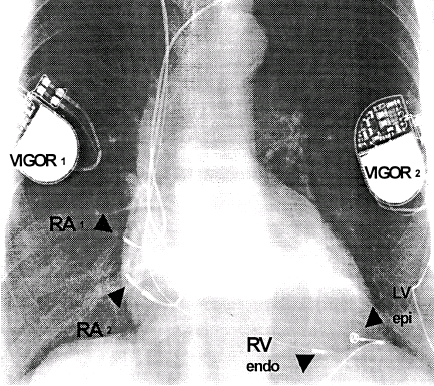
FIG.1 Stimolazione endocardica destra ed epicardica sinistra con doppio dispositivo.
TAB. 1 Indicazioni alla terapia di resincronizzazione in assenza di blocco di branca sinistra.
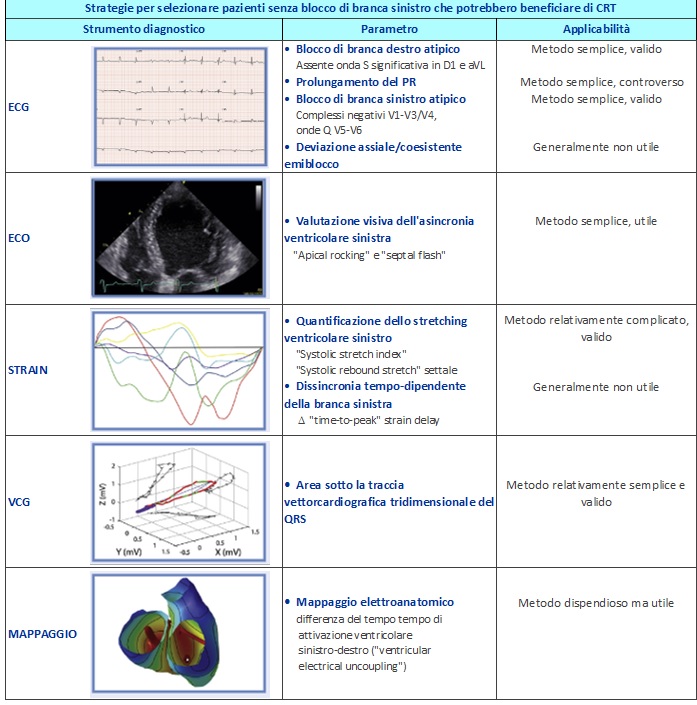
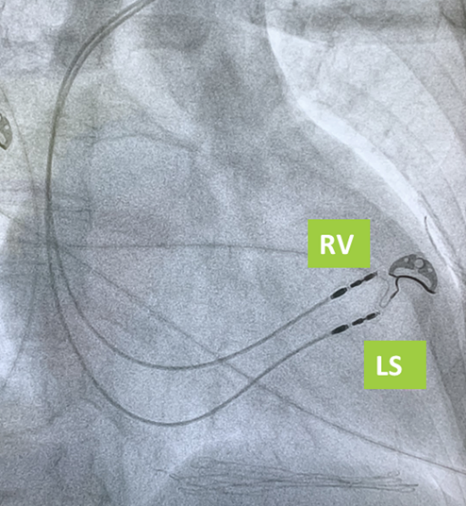
FIG.2 Terapia di modulazione della contrattilità cardiaca.